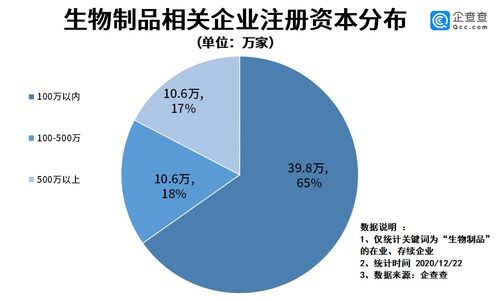
國家藥品監督管理局正式發布了新版《生物制品管理辦法》,標志著我國生物制品行業管理邁入更加科學化、規范化的新階段。該辦法對生物制品的研發、生產、流通與監管全鏈條進行了系統性優化與明確要求,旨在保障藥品安全有效、促進產業高質量發展。在這一政策利好的強勁驅動下,我國生物制品相關企業展現出前所未有的活力,市場響應積極,企業注冊量顯著攀升。
據最新市場數據顯示,本年度(截至當前統計周期)我國新增注冊的生物制品相關企業數量同比實現了17.2%的顯著增長。這一增長數據直觀地反映出,新管理辦法的出臺為市場注入了強大的信心,吸引了更多資本與技術力量進入生物醫藥這一戰略性新興產業領域。企業注冊熱潮不僅體現在數量上,更在質量上有所提升,新進入者多聚焦于創新藥研發、高端生物類似物、細胞與基因治療等前沿方向,推動了行業整體結構的優化升級。
從企業管理角度看,新版《生物制品管理辦法》對企業提出了更高、更具體的要求,這既是挑戰,也是轉型升級的契機。辦法強化了全過程質量控制體系,要求企業建立覆蓋研發、臨床試驗、生產、上市后監測的全生命周期質量管理體系。這促使企業必須加大在質量管理體系(QMS)建設、信息化追溯系統以及專業人才隊伍上的投入,從而提升內部管理的精細化與合規性水平。
辦法鼓勵創新并明確了相關支持路徑,例如對臨床急需的創新生物制品設立了優先審評審批通道。這引導企業將管理重心從單純的規模擴張轉向以研發創新為核心驅動力的發展模式。企業管理層需要更加注重戰略規劃,優化研發管線管理,加強知識產權布局,并積極尋求產學研醫合作,以抓住政策機遇。
在供應鏈與流通管理方面,辦法對生物制品的儲存、運輸條件(尤其是冷鏈)提出了嚴格規定。相關企業必須升級其物流管理體系,投資建設或合作依托于符合GSP標準的冷鏈設施,確保產品從出廠到使用終端全程處于可控的溫控環境,這直接關系到企業的運營成本管理與市場競爭力。
隨著《生物制品管理辦法》的深入實施和監管環境的持續完善,預計我國生物制品行業將迎來一輪持續的“提質增量”發展期。主動適應新規、強化內部合規管理、聚焦創新與質量,將是贏得市場競爭的關鍵。17.2%的企業注冊增長數據也預示著行業競爭將更加激烈,兼并重組與專業化分工或將加速,最終推動我國從生物制品大國向強國穩步邁進。